自己免疫性溶血性貧血の検査

自己免疫性溶血性貧血(autoimmune hemolytic anemia:AIHA)
に関する検査を依頼される先生方へ
検査内容
- ■CBC 検査(赤血球数、白血球数、血小板数、ヘモグロビン量、ヘマトクリット値、赤血球恒数(MCV、MCH、MCHC)、網赤血球数)
- ■フローサイトメトリー(FCM 法)による赤血球結合IgG 定量検査
- ■直接クームス試験(試験管法:IgG、C3b,C3d、ゲルカラム法:広範囲、IgG、C3d)
- ■PBS 洗浄後直接クームス試験(IgG)、PBS 洗浄後陰転時:LISS 洗浄後直接クームス試験(IgG)
- ■自己凝集陽性の場合:2ME 処理自己赤血球での直接クームス試験(試験管法:IgG、C3b,C3d、ゲルカラム法:IgG)
検査内容は患者様により変動します。
なお、当検査は診療の補助を目的とした検査であることから、必ずしも診断のための質の担保がなされているものではないことにご留意ください。
【お知らせ】
検査試薬の販売中止のため、直接クームス試験 試験管法:IgA, IgM および2ME処理自己赤血球での直接クームス試験(試験管法)IgA, IgMにつきましては、2023年3月30日受付をもちまして、検査中止とさせていただきました。
検査依頼方法
検査依頼は、福山臨床検査センターへご連絡いただき、検体送付日をご予約ください。
月〜木曜日着で受託しております。但し、祝日等が入りますと受託できない日がございますので、必ず事前にご連絡をお願いいたします。
検体
・全血 2mL×2 本(抗凝固剤EDTA-2K またはEDTA-2Na)
頻回に輸血されている場合は、輸血直前の検体をお送りください。患者赤血球を用いた検査となりますので、血漿や血清のみの検査はお受けできません。
送付方法
・検体送付の費用につきましては、依頼医療機関でご負担をお願いいたします。
・全血を冷蔵にてお送りください。(検体が凍らないようにご配慮ください。検体チューブが保冷剤に直接触れていますと凍結の恐れがあります。凍結した検体は検査ができなくなりますのでご注意ください。)
・採血後すみやかに発送をお願いいたします。平日 月~木曜日の午前中到着指定でお願いいたします。
・当社検体到着時に検体識別を確実にするため、各検体には依頼書にご記入いただいた患者様のID番号と生年月日のご記入をお願いいたします。
貴施設で貼られるラベルに既にこれらの記載がある場合は必要ありません。どちらか一方だけの場合は、記載のない方をご記入ください。
検査報告
検査結果のご報告までの日数は検体到着後7〜10 日程度です。検査結果は、結果解釈のコメントを付記して福山臨床検査センターより郵送にてご報告させていただきます。結果解釈のご相談があればお問い合わせフォームよりお問い合わせください。
ご請求
検査結果報告書発送月の翌月上旬に請求書を送付いたしますので、所定の銀行へお振り込みにてお支払いください。
*請求書は施設様宛に発行いたします。お振り込みについては被験者様へ依頼するのでなく、施設様から行っていただけます様お願いいたします。
*振り込み手数料につきましてはご負担をお願い申し上げます。
ご依頼・お問合せ・検体送付先
ご依頼・お問い合わせ・検体送付先が変更になりました(2024年6月17日受付以降)
2024年6月17日受付より、ご依頼・お問い合わせ・検体送付先を下記のように変更させていただきました。何卒、ご理解の程、宜しくお願い致します。
※お問い合わせについては、以下のフォームより必要事項をご記入のうえ、メールにてご連絡ください。当方より折り返し連絡させていただき、検体の採取、送付方法、検査費用などのご案内をさせていただきます。ご不明な点については遠慮なくお問い合わせください。なお、依頼元は医療機関に限らせていただきます。
ご依頼・お問い合わせ連絡先
株式会社 福山臨床検査センター 本社営業部 (溶血性貧血検査担当)
Tel: 084-921-0120
受付時間 日曜・祝日・祭日を除く平日 9:00~17:00
検体送付先
株式会社 福山臨床検査センター 水呑分室(みのみぶんしつ)
〒720-0832 広島県福山市水呑町456-2
Tel:084-920-5750
(平日 月~木曜日の午前中の到着指定で発送をお願いいたします)
お知らせ
検体は月~木曜日の午前中の到着にて受託しております。祝日等が入りますと受託出来ない日がございます。必ず事前にご連絡をお願いいたします。
特に北海道・東北・沖縄より発送される場合は、到着日の遅れが多々生じております。配送希望日を伝票に明記の上、配送業者様に到着日を必ず確認していただきますようお願いいたします。
検査を依頼される前に以下のチェックをお勧めいたします
- 1.ハプトグロビンは感度以下ですか?(正常値以上の場合は溶血がない可能性が高い) なお、巨赤芽急性貧血(VitB12 欠乏など)では、骨髄での無効造血により、ハプトグロビンが低下することがあります。また、高度の炎症がある場合はハプトグロビンが増加して陰性化しない場合もあります。
- 2.破砕赤血球は検出されていませんか?(非免疫性溶血が疑われます)
さらに血小板減少がある場合は、TTP が疑われますので、ADAMTS13 活性測定などをご検討ください。
【注意】血小板減少があり、クームス陰性Evans 症候群を疑った場合は、破砕赤血球がなくともTTP の可能性はあります。
「423 例のTTP 患者の84 例(20%)に初期診断の誤り(ITP と誤診)があり、女性、軽症貧血、DAT 陽性、破砕赤血球少数~陰性が誤診のリスク因子であった。破砕赤血球を認めないDATが弱陽性の溶血患者であっても、血小板減少と特に臓器障害を伴っている場合は、TTP も念頭にADAMTS13 活性測定などをおこなう必要がある。」Am J Hematol. 2017;92:381–387.。 - 3.クームス試験陰性が試験管法なら、カラム法を試してみる。(感度が上がります)
- 4.*血色素異常症(異常ヘモグロビン症、サラセミア)検査リンク>>
- 5.*先天性赤血球酵素異常症検査リンク>>
寒冷凝集素の温度作動域の検査はお受けしておりません。
参考資料
AIHAの概要

無料ダウンロード可
クームス陰性(温式)AIHA の概要と診断方法
クームス陰性AIHA はAIHA の5-10% で認められ、診断や治療の遅延が危惧されます。原因としては、クームス試験感度以下の赤血球結合IgG 自己抗体、低親和性IgG 自己抗体、IgM/IgA 自己抗体の3 種があり、それぞれの検出検査が診断に有用です。
クームス試験感度以下の赤血球結合IgG自己抗体が主要な原因とされており、フローサイトメトリー(FCM) 法による赤血球結合IgG 定量が診断の補助検査として有用で、ステロイド治療を開始する根拠ともなります。
*フローサイトメトリー(FCM) 法による赤血球結合IgG 量の正常値:5.5-16.0
MFID(Mean Fluorescence intensity difference)
1.高値の場合
免疫性溶血性貧血が疑われます。
治療への反応性や臨床経過と併せて、赤血球結合IgG 量の変化をフォローされますと、診断の確実性が増し、治療効果の判定や再燃のチェックも可能かと思われます。
また、溶血の再燃・増悪など病状の変化した際などには、再検査の依頼もご検討ください。
不規則抗体があれば、輸血療法後にその影響で高値になっている可能性はあります(同種免疫性溶血)。不規則抗体に対応した適合輸血であれば可能性は低いと思われます。
2.正常値の場合
免疫性溶血は否定的です。
免疫抑制療法(ステロイドなど) 中や治療後であれば、治療による正常化は否定できません(治療反応性なども参考にしてご判断ください)。
採血時に溶血が軽快している場合は、一過性のAIHA の治癒期である可能性は否定できません。
輸血療法後の場合は、正常赤血球の混入のため正常化している可能性はあります。
カラム法クームス試験が陽性の場合は、低親和性IgG 自己抗体の関与が疑われます。
補体クームス試験が陽性の場合は、CAD やPCH についてもご検討ください。
3.低値の場合
網赤血球が増加している非免疫性溶血患者では、結合IgG 量は低下していることがあります。
4.注意点
抗IgA/IgM クームス試薬が日本では入手できなくなったため、クームス陰性AIHA 5%程度を占めるIgA/IgM 型AIHA については、当検査センターの検査が陰性であっても否定できないことにご留意ください。
以前行われていたRIA 法による検査と異なり、現在行われているFCM 法による検査では、低親和性IgG 自己抗体は概ね通常の赤血球結合IgG として検出されます。
FCM 法が正常値であってもカラム法クームス試験が陽性の場合が稀にあり、低親和性IgG 自己抗体の関与が疑われます。
クームス試験において陰性コントロールが陽性の場合は、自己凝集が認められ、通常IgM 自己抗体の関与が疑われます。
5.参考文献
大峠ふくみ, 山城安啓, 他: フローサイトメトリーによる赤血球結合IgG 測定法の開発. 医学検査71(1):37-44, 2022.
自己免疫性溶血性貧血診療の参照ガイド(令和4 年度改訂版). 特発性造血障害研究班
http://zoketsushogaihan.umin.jp/file/2022/Autoimmune_hemolytic_anemia.pdf
クームス陰性自己免疫性溶血性貧血. 別冊日本臨牀血液症候群(第3 版) I, 353-357, 日本臨牀社, 2023.
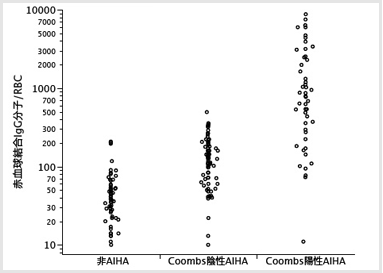
赤血球結合IgG 量(RIA 法):正常、クームス陰性AIHA、クームス陽性AIHA、診断カットオフ値
Coombs 試験が陽性となるには赤血球1 個あたり250 分子以上のIgG が必要であり、健常人の赤血球上に平均33±13(SD)個のIgG 分子が存在している(図1)。
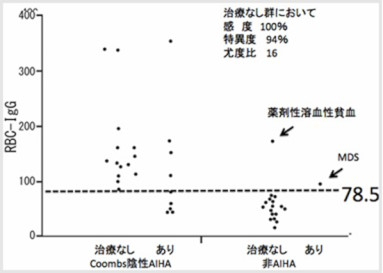
Coombs 陰性溶血性貧血140 例において、Coombs 陰性AIHA 診断における赤血球結合IgG 量の感度・特異度・尤度比を算出しROC(receiveroperating characteristic)曲線からカットオフ値を求めると、カットオフ値83 以上で感度70%、特異84%、尤度比4.8 であった。
2006 年度依頼Coombs 陰性症例41 例中、治療前の31 例についてみると、カットオフ値79 以上で感度100%、特異度94%、尤度比16 であった。Coombs 陰性溶血性貧血を診る際には、治療前の赤血球結合IgG 定量がCoombs 陰性AIHA 診断において高い有用性を示すと考えられる(図2)。
【参考文献】
Cut-off value of red-blood-cell-bound IgG forthe diagnosis of Coombs-negative autoimmune hemolyticanemia. Am J Hematol. 2009;84(2):98-101.
Characterization of direct antiglobulin test-negative autoimmune hemolyticanemia: A study of 154 case.
Am J Hematol.2013 88(2):93-96
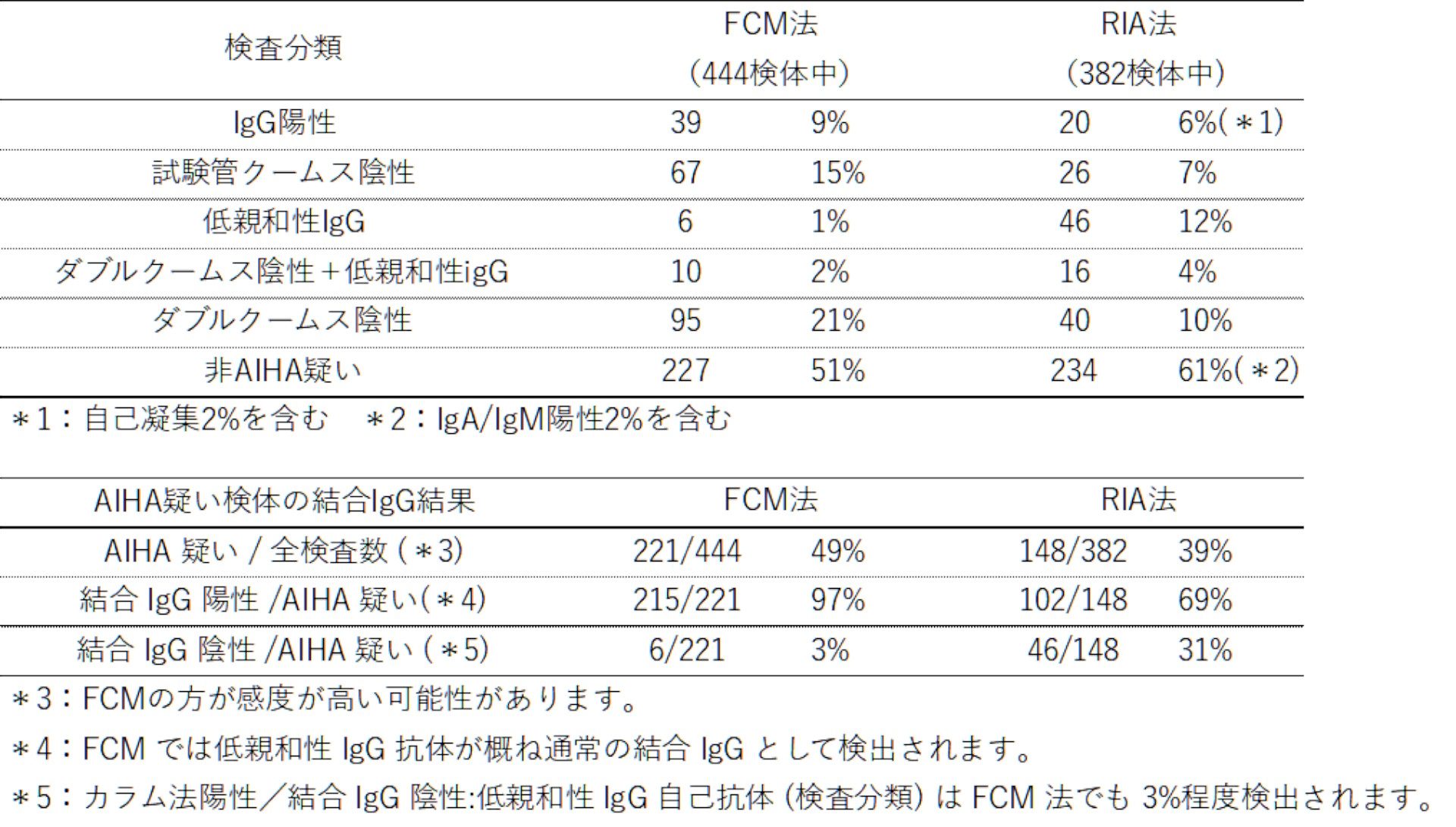
クームス陰性AIHA の診断アルゴリズムによる検査分類と臨床診断(RIA 法)
クームス陰性AIHA は、上記の3 つのDAT 陰性化機序を考慮した検査法により、6 つのサブグループ(試験管クームス陰性AIHA、ダブルクームス陰性AIHA、低親和性IgG 型AIHA、IgA/IgM 型AIHA、低親和性IgM 型AIHA、「臨床的に診断されたクームス陰性AIHA」)に分類できる。(図3:クームス陰性AIHA の診断アルゴリズム) いずれの検査も陰性であれば「非AIHA 疑い」に分類するが、「非AIHA 疑い」症例であっても、非免疫性溶血性貧血が否定され、免疫抑制療法が有効な場合は「臨床的に診断されたクームス陰性AIHA」に分類される。
2015 年から2019 年に検査依頼のあった382 例の検査分類は、自己凝集2%、IgG 陽性4%、試験管クームス陰性7%、低親和性IgG16%、ダブルDAT 陰性10%、IgA/IgM 陽性2%、低親和性IgM0.3%、非AIHA 疑い59%であった。
検査から1 年後に主治医により臨床診断されたクームス陰性AIHA126 例では、試験管クームス陰性AIHA 16%、低親和性IgG 型AIHA 35%、ダブルクームス陰性AIHA 25%、IgA/IgM陽性AIHA 6%、低親和性IgM 型AIHA 0.8%、「臨床的に診断されたクームス陰性AIHA」(検査分類の偽陰性)17%であった。本診断アルゴリズムのAIHA 診断感度と特異度は共に85%であったが、治療前に検査を行った症例(279 例)に限定すると、「臨床的に診断されたクームス陰性AIHA」(検査分類の偽陰性)は4%となり、感度は97%、特異度は84%であった。従って、クームス陰性AIHA を疑う場合は、治療前に専門機関に検査を依頼することが推奨される。
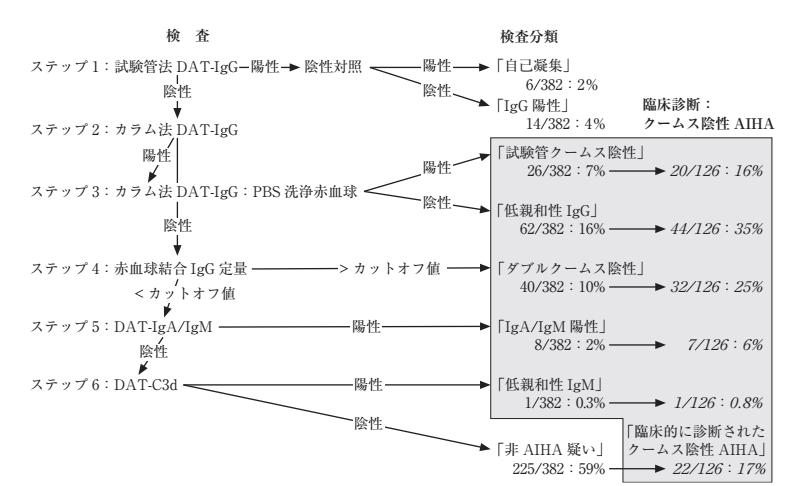
図3 クームス陰性AIHA の診断アルゴリズムによる検査分類と臨床診断(RIA 法)(クームス陰性自己免疫性溶血性貧血. 別冊日本臨牀血液症候群(第3 版) I, 353-357, 日本臨牀社, 2023.より引用)
【参考文献】
Diagnostic algorithm for classification and characterization of direct antiglobulin test-negativeautoimmune hemolytic anemia with 1-year clinical follow-up. Transfusion 62:205-216,2022.
赤血球結合球IgG 量のクームス陰性AIHA 診断カットオフ値(FCM 法)
赤血球結合IgG 定量は、以前はRIA 法(カットオフ値:78.5 IgG 分子/ 赤血球) で行われていたが、現在はフローサイトメトリー法(カットオフ値:16.0 MFID(Mean Fluorescence intensity difference), 正常値5.5-16.0) により、福山臨床検査センターで行われている。
(https://www.fmlabo.com/service/erythrocyte/aiha/)(図4)
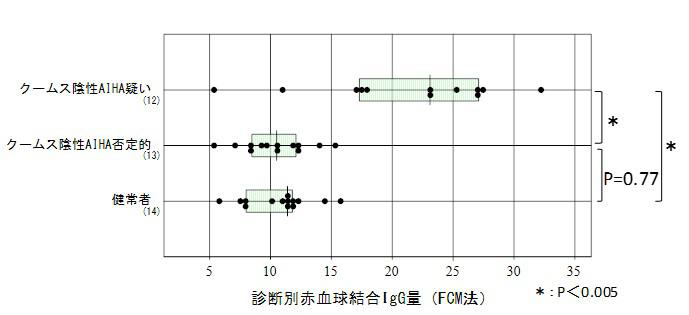
図4 赤血球結合球IgG 量のクームス陰性AIHA 診断カットオフ値(FCM 法)
【参考文献】
大峠ふくみ, 山城安啓, 他: フローサイトメトリーによる赤血球結合IgG 測定法の開発. 医学検査71(1):37-44, 2022.
自己免疫性溶血性貧血診療の参照ガイド(令和4 年度改訂版). 特発性造血障害研究班, 2023.
http://zoketsushogaihan.umin.jp/file/2022/ Autoimmune_hemolytic_anemia.pdf

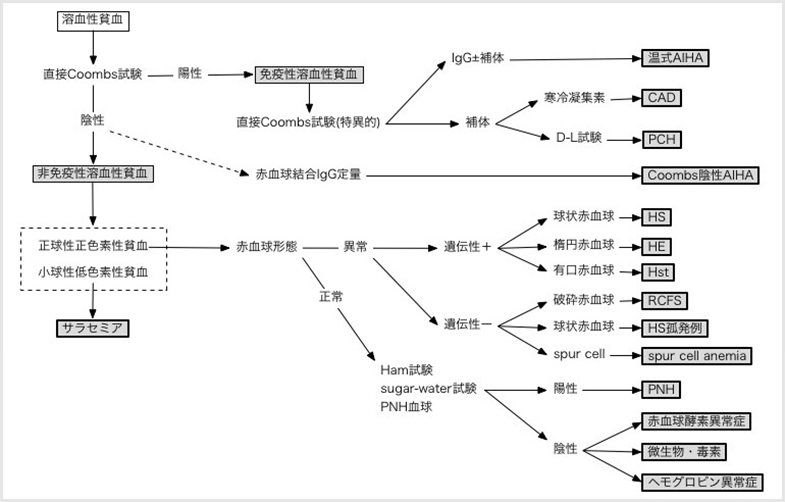
溶血性貧血の診断フローチャート
血液検査や臨床症状から溶血性貧血を疑った場合は、直接Coombs 試験を行い、陽性の場合は特異的Coombs 試験で赤血球上のIgG と補体成分を確認する。
補体のみ陽性の場合は、寒冷凝集素やPCH の鑑別のため、寒冷凝集素価測定とDL 試験をおこなう。(内科疾患の診断基準・病型分類・重症度溶血性貧血. 内科2015;115:1304-1307.より引用)
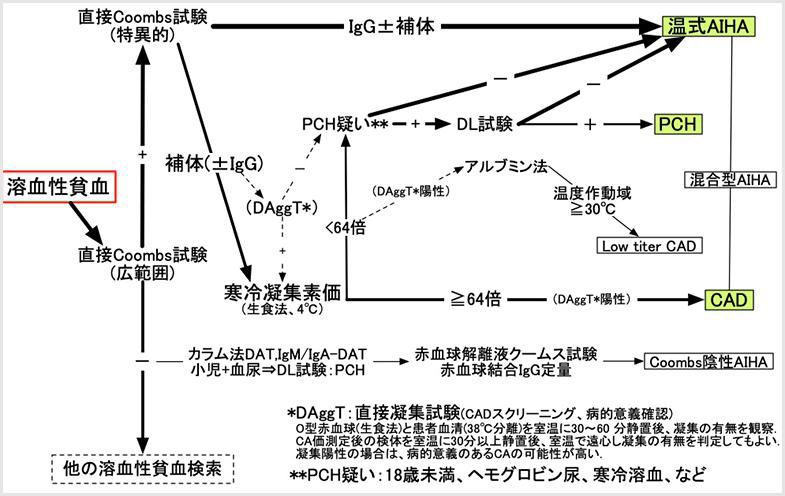
免疫性溶血性貧血診断のフローチャート
2017 年に英国血液学会が発表した免疫性溶血性貧血の診断フローチャート*では、特異的直接Coombs 試験でIgG 陽性の場合は温式AIHA を疑い、C3d(±IgG)の場合はCAD を疑って室温での直接凝集試験(direct agglutination test:DAggT)を行うことが提唱されている。
DAggT 陽性かつ寒冷凝集素価が64 倍以上であればCAD と診断し、DAggT 陰性の場合は病的意義のない寒冷凝集素として取り扱われる。DAggT や寒冷凝集素価測定に用いる血清は37℃以上での分離が重要であると強調されている。
また、直接Coombs 試験陰性であってもAIHA が疑われる場合は、試験管法に加えてカラム法によるCoombs 試験再検やIgM/IgA 特異的Coombs 試験、ヘモグロビン尿のある小児例ではDonath-Landsteiner 試験、赤血球解離液での間接Coombs 試験の施行が推奨されている。
低力価寒冷凝集素症(low titer CAD)については, 英国血液学会のフローチャートに記載はないが, わが国からの報告が散見されることから残している. Low titer CAD 診断においては, Coombs 陰性(温式)AIHA の可能性も考慮すべきである。( “貧血”の読み方・捉え方2.実践編:貧血の検査データの読み方症例③(溶血性貧血). Medical Technology 2018.)
* The diagnosis and management of primary autoimmune haemolytic anaemia. Br. J.
Haematol.,176(3):395-411, 2017.
・赤血球解離液クームス試験:グリシン塩酸/EDTA 解離法→ゲルカラム法IAT
Does a negative direct antiglobulin test exclude warm autoimmune haemolytic anaemia? A prospective study of 504 cases. Br J Haematol. 132(5):655-6, 2006.
‘ゲルカラム法DAT 陰性患者の3%にAIHA 診断可能’
・直接凝集試験Direct Agglutination Test (DAggT)
Cold antibody autoimmune hemolytic anemias. Blood Rev. 22(1):1-15, 2008.
患者血清(寒冷凝集素価検査時と同様に37℃で分離)2 滴+3%正常O 型赤血球(生食法)1 滴、室温(または20℃)で30-60min 静置後、凝集判定→陰性ならCAD は否定的。検査会社で受注していないため、自前の検査室で行う必要がある。
なお、DAggT を新たに行う代わりに、寒冷凝集素価を4℃で測定した検体を、室温に30 分以上静置し、遠心後に凝集の有無を判定すれば、原理的には同様な結果が得られると思われる。
すなわち、室温で1 倍以上の凝集の残存や溶血が認められる場合は病的意義のある可能性が高く、凝集が認められなくなる場合は病的意義は低いと判断する。
・患者赤血球結合IgG の定量:フローサイトメトリー
寒冷凝集素温度作動域測定マニュアル
寒冷誘発性の溶血を認め、直接クームス試験で補体成分(C3d)が検出される場合は、冷式AIHA を疑い、寒冷凝集素価(4℃)ならびにDonath-Landsteiner 試験をおこなう。寒冷凝集素が64 倍以上であれば、寒冷凝集素症(Cold agglutinin disease: CAD)の可能性があり、悪性腫瘍や感染症が否定されるとCAD と診断される。基礎疾患が認められる2 次性の場合はCAS(Cold Agglutinin Syndrome: CAS)と診断する。冷式抗体の検査では、採血時から検体を37℃-38℃に保温して血清分離を行うことが重要である。
How I manage patients with cold agglutinin disease. Br J Haematol 181(3):320-330, 2018.
4℃で最大の凝集素価を示し、30℃以上まで凝集が認められれば、病的意義のある寒冷凝集素と判断される。凝集素価よりも温度作動域の拡大のほうが、溶血症状と関係が強いと言われている。
* 低力価寒冷凝集素症:low titer cold agglutinin disease
寒冷凝集素は、30℃以上で凝集活性がある場合には病的意義があるとされる。スクリーニング検査として、患者血清(もしくは血漿:37~40℃下で分離)と生食(もしくは22%アルブミン液)に懸濁したO 型赤血
球を混和し、室温(20~25℃)に30-60 分放置後、遠心し凝集を観察する。凝集が認められない場合は病的意義のない寒冷凝集素と考えられる。
凝集が見られた場合には、さらに温度作動域の検討を行う。37℃、30℃、室温(20~ 25℃)、4℃での凝集素価を生食法(もしくはアルブミン法)で測定する。すなわち、生食(もしくは22%アルブミン液) で倍々希釈した患者血清と生食(もしくは22%アルブミン液)で3%に調整したO 型赤血球を混和し、37℃で30分静置後、遠心し凝集を観察する。凝集の認められた最高希釈倍率を37℃での寒冷凝集素価とする。その後、30 度に30 分静置後、同様に凝集素価を測定する。室温、4℃でも同様に凝集素価を測定する。
アルブミン法では、生食の代わりに22%アルブミン液を用いて血清と赤血球の希釈を行う。
寒冷凝集素価の上昇が軽度(<1000 倍) であったり、正常範囲内であっても、寒冷曝露に伴う溶血が疑われる場合は、温度作動域の検討を行うと、30℃以上での凝集が認められることがあり、病的な意義のある寒冷凝集素と判断される。低力価であり温度作動域が拡大している症例(低力価寒冷凝集素症)では、ステロイド治療が有効な症例が報告されている。生食法に加えてアルブミン法を行うと検出感度が高くなり、凝集素価の上昇も認められることがある。
Low-titer cold-hemagglutinin disease:Mechanism of hemolysis and response to corticosteroids. N Engl J
Med 296:1490-1494, 1977. 26.
Steroid-responsive idiopathic cold agglutinin disease: a case report. Acta Haematol 81:166-168, 1989.
寒冷凝集素:温度作動域測定マニュアル
検体
患者血清(又は血漿)5ml:37-40℃で分離
O型健常人(EDTA もしくはヘパリン)血液5ml(検査血球として使用)
寒冷凝集素スクリーニング検査
寒冷凝集素は、30℃以上で凝集活性がある場合に病的意義があるとされる。
①患者血清(37~40℃下で分離)
②O 型赤血球をPBS で4 回洗浄後、PBS(もしくは22%アルブミン液)で3%濃度に懸濁
③1.血清2 滴と2.血球1 滴を混和、室温(20~25℃)に30-60 分放置
④遠心後、凝集を観察する。
*凝集が認められない場合は、病的意義のない寒冷凝集素とし終了。
*凝集が見られた場合には、さらに温度作動域の検討を行う。
寒冷凝集素温度作動域測定
①37℃、30℃、室温(20~25℃)、4℃での凝集素価を生食法(もしくはアルブミン法)で測定する。
②患者血清を生食(もしくは22%アルブミン液)で倍々希釈
③O 型赤血球を生食(もしくは22%アルブミン液)で3%に調整
④2.血清2 滴と3.血球1 滴を混和、37℃で30-60 分静置
⑤遠心後速やかに37℃恒温槽に静置し凝集を観察する。(もしくは、2 時間静置後凝集を観察する)
⑥* 凝集の認められた最高希釈倍率:その温度での寒冷凝集素価
⑦その後、30℃に30-60 分静置後、同様に凝集素価を測定する。
⑧室温、4℃(30-60 分またはオーバーナイト)でも同様に凝集素価を測定する。
⑨* アルブミン法では、生食の代わりに22%アルブミン液を用いて血清と赤血球の希釈を行う。
⑩* 寒冷凝集素スクリーニング検査ならびに温度作動域の測定は、現在外注で依頼できる検査機関がないことから、自前の検査室で行う必要がある。
Serological Diagnosis and Characterization of the Causative Autoantibodies.In: Chaplin H, ed.
Immune Hemolytic Anemias (Methods in Hematology), Churchill Livingstone;1985.p27-35.
The serologic Investigation of autoimmune hemolytic anemia. In: Petz LD,Garratty G, editors.
Immune Hemolytic Anemias. Philadelphia: Churchill Livingstone; 2004. pp 220–222.
Donath-Landsteiner 試験法
Donath-Landsteiner 抗体(二相性溶血素、DL 抗体)の検出は、現在外注で依頼できる検査機関がないことから、自前の検査室で行う必要がある。血液検体としてPNH 血球や酵素処理血球を用いると感度が高くなるとされている。患者血液で行う直接DL 試験*と患者血清中のDL 抗体を証明する間接DL 試験**がある。直接法は簡易だが補体が生体内で消費されると陰性となりやすく、間接法の方が感度は高い。
*直接DL 試験
患者血液5ml(抗凝固剤未添加)2本採血し、それぞれ0℃、37℃に30 分静置後、2 本とも37℃30 分静置し、1000g,5 分遠心し、冷却分のみ溶血が認められれば、DL 抗体陽性とする。
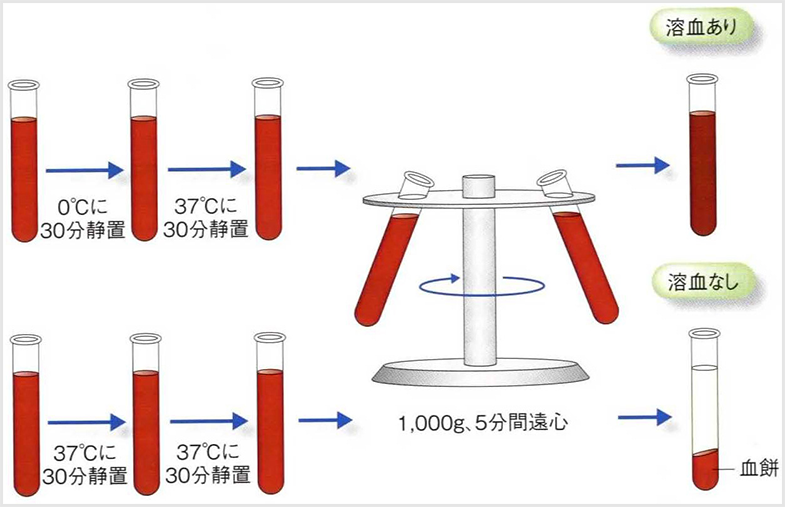
(専門医に紹介すべき貧血自己免疫性溶血性貧血. Mebio 28(9):72-81,2011.)
**間接DL 試験
37℃で分離した患者血清を準備。2 本の試験管に10%O 型洗浄赤血球浮遊液1 滴と患者血清5 滴と新鮮正常血清を5 滴を入れる(試験用)。別の2 本の試験管に10%O 型洗浄赤血球浮遊液1 滴と新鮮正常血清を10 滴加える(コントロール用)。試験用とコントロール用各1 本ずつを0℃30 分静置後、37℃30 分静置。他の試験用とコントロール用各1 本ずつを37℃1 時間静置。4 本の試験管を1000g,5分遠心し、冷却した試験用のみ溶血していればDL 抗体陽性とする。
Serological Diagnosis and Characterization of the Causative Autoantibodies.In: Chaplin H, ed.
Immune Hemolytic Anemias (Methods in Hematology), Churchill Livingstone;1985.p35-37.
The serologic Investigation of autoimmune hemolytic anemia. In: Petz LD,Garratty G, editors.
Immune Hemolytic Anemias. Philadelphia: Churchill Livingstone; 2004. pp 223–224.
混合型AIHA
温式AIHA(Coombs 陰性AIHA も含む)と寒冷凝集素症(低力価CAD を含む)が合併している場合は、混合型AIHA の診断となる(Coombs 陰性AIHA と寒冷凝集素症の合併も広義の混合型AIHA といえる)。


